

在现代生物技术与结构生物学研究中,重组蛋白的表达与纯化是将遗传信息转化为可解析分子实体的核心环节。对于以 X 射线晶体学或冷冻电镜为目标的研究而言,获得蛋白并不意味着实验成功,真正的目标是获得构象均一、化学纯度高且保持天然折叠状态的样品。从这一视角看,蛋白制备并非简单的操作流程,而是一个需要精确调控能量状态与分子相互作用的系统工程。
▌基因设计与翻译动力学的分子基础
重组蛋白制备的起点是基因序列设计。不同物种在同义密码子的使用频率上存在显著差异,这种密码子偏好性直接影响翻译延伸的动力学行为。当外源基因中富含宿主的稀有密码子时,核糖体容易发生停滞,导致新生肽链在未完成折叠前暴露疏水区域,从而增加错误折叠或降解的风险。
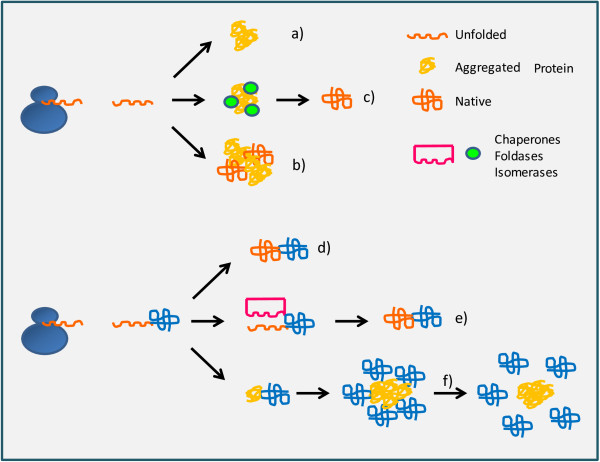
通过密码子优化,使编码序列与宿主细胞的 tRNA 丰度分布相匹配,可以维持相对平稳的翻译速率,为共翻译折叠提供时间窗口。此外,启动子强度与诱导条件同样影响蛋白质量。过快的合成速率可能使分子伴侣系统不堪重负,促使聚集体形成。因此,从分子层面看,表达效率与可溶性之间始终存在需要平衡的动力学关系。
▌细胞裂解与粗提液稳定性控制
表达结束后,目标蛋白仍处于复杂的细胞环境中,必须通过裂解步骤将其释放。无论采用机械破碎还是酶解方式,裂解都会瞬间打破细胞内的空间隔离,释放大量内源性蛋白酶。这些蛋白酶可迅速切割目标蛋白的柔性区段,是影响样品完整性的主要威胁之一。
因此,裂解过程通常需要在低温条件下进行,并辅以广谱蛋白酶抑制剂以降低非特异性降解。同时,基因组 DNA 的释放会显著提高溶液黏度,影响后续层析效率,通过核酸酶降解 DNA 并结合高速离心澄清裂解液,是获得稳定粗提液的关键前处理步骤。
▌亲和层析:特异性捕获的化学本质
纯化流程的第一阶段通常是捕获步骤,其目标是在复杂背景中快速富集目标蛋白。亲和层析正是基于分子识别原理实现这一目的。以 His 标签体系为例,组氨酸侧链与金属离子之间形成可逆配位键,使目标蛋白能够在适当条件下选择性结合固定相。通过竞争性洗脱破坏配位相互作用,可以在较小体积内获得高纯度蛋白。其他亲和体系则依赖不同形式的分子识别,但其共同点在于利用特异性相互作用实现选择性富集,从而显著降低体系复杂度。
▌离子交换层析与电荷分离机制
在捕获之后,离子交换层析常用于进一步提高样品纯度。该技术基于蛋白质表面电荷分布的差异进行分离,而这一分布又由蛋白的等电点及局部结构决定。当缓冲液 pH 与蛋白 pI 存在偏差时,蛋白可与带相反电荷的树脂发生静电吸附。通过逐步提高盐浓度,可以有序削弱静电相互作用,使不同蛋白按电荷特性依次洗脱。由于电荷分布对构象变化和翻译后修饰高度敏感,离子交换层析在区分微小异构体方面具有独特优势。
▌分子筛层析与单分散性评估
尺寸排阻层析通常是纯化流程的终点,其功能不仅在于分离,更在于质量评估。SEC 依据分子流体力学体积进行分离,能够有效区分单体、寡聚体与聚集体。在理想状态下,目标蛋白应表现为对称且尖锐的单峰,反映其处于单分散状态。结合 SDS-PAGE 可判断峰对应的分子组成,而动态光散射等技术则可进一步评估溶液中粒径分布的均一性。对于结构生物学研究而言,单分散性是样品能否进入结晶或冷冻电镜分析的基本门槛。
总体来看,重组蛋白制备是一个将分子生物学、胶体化学与物理分离技术深度融合的过程。从基因层面的翻译动力学调控,到层析过程中的分子识别与物理筛选,每一步都直接影响最终样品的质量。只有在理解这些底层机制的基础上,才能稳定获得满足高分辨率结构研究要求的蛋白样品。